- Arginin
-
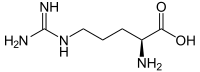
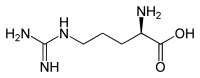
Strukturformel 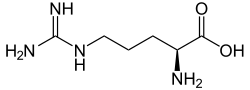
L-Arginin Allgemeines Name Arginin Andere Namen - L-Arginin, Arg, R
- (S)-Arginin
- α-Amino-δ-guanidinvaleriansäure
- Abkürzungen:
- Arg (Dreibuchstabencode)
- R (Einbuchstabencode)
Summenformel C6H14N4O2 CAS-Nummer - 74-79-3 (L-Enantiomer)
- 157-06-2 (D-Enantiomer)
PubChem 6322 ATC-Code DrugBank DB00125 Kurzbeschreibung weißer Feststoff[1]
Eigenschaften Molare Masse 174,20 g·mol−1 Aggregatzustand fest
Dichte 0,7 g·cm−3[1]
Schmelzpunkt pKs-Wert Löslichkeit gut in Wasser (150 g·l−1 bei 20 °C)[1]
Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 319 EUH: keine EUH-Sätze P: 305+351+338 [3] EU-Gefahrstoffkennzeichnung [1]
Xi
ReizendR- und S-Sätze R: 36 S: 26 LD50 5110 mg·kg−1 (Ratte, peroral)[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. L-Arginin, abgekürzt Arg oder R, ist eine proteinogene α-Aminosäure. Für den Menschen ist sie semiessentiell. Der Name leitet sich vom lateinischen Wort argentum (Silber) ab, da die Aminosäure zuerst als Silber-Salz isoliert werden konnte. Diese Aminosäure hat den höchsten Masseanteil an Stickstoff von allen proteinogenen Aminosäuren. Im Dreibuchstabencode wird L-Arginin mit Arg und im Einbuchstabencode als R abgekürzt.
Inhaltsverzeichnis
Vorkommen
L-Arginin ist weit verbreitet. Die folgenden Beispiele geben einen Überblick über Arginingehalte und beziehen sich jeweils auf 100 g des Lebensmittels, zusätzlich ist der prozentuale Anteil von Arginin am Gesamtprotein angegeben.[4]
-
Lebensmittel Gesamtprotein Arginin Anteil Schweinefleisch, roh 20,95 g 1394 mg 6,7 % Hähnchenbrustfilet, roh 21,23 g 1436 mg 6,8 % Lachs, roh 20,42 g 1221 mg 6,0 % Hühnerei 12,57 g 820 mg 6,5 % Kuhmilch, 3,7 % Fett 3,28 g 119 mg 3,6 % Pinienkerne 13,69 g 2413 mg 17,6 % Walnüsse 15,23 g 2278 mg 15,0 % Kürbiskerne 30,23 g 5353 mg 17,7 % Erdnuss, geröstet 23,68 g 2832 mg 11,9 % Weizen-Vollkornmehl 13,70 g 642 mg 4,7 % Mais-Vollkornmehl 6,93 g 345 mg 5,0 % Reis, ungeschält 7,94 g 602 mg 7,6 % Buchweizenkörner 13,25 g 982 mg 7,4 % Erbsen, getrocknet 24,55 g 2188 mg 8,9 %
Eigenschaften
Arginin ist eine α-Aminosäure mit einer Guanidin-Funktionalität in der Seitenkette. Gemeinsam mit L-Lysin und L-Histidin gehört L-Arginin in die Gruppe der „basischen“ Aminosäuren oder Hexonbasen. Diese besitzen eine basische Gruppe, hier eine Guanidinogruppe, die im Neutralbereich stets protoniert (positiv geladen) ist. Arginin ist gut in Wasser löslich und reagiert (durch Bindung von Protonen) alkalisch. Die Guanidin-Gruppe ist sowohl im sauren und neutralen, als auch im schwach basischen Milieu protoniert und trägt eine positive Ladung, die zwischen den Aminogruppen delokalisiert ist. Proteine, die L-Arginin enthalten, werden durch diese Ladung hydrophiler, also wasserlöslicher.
Arginin liegt überwiegend als „inneres Salz“ bzw. Zwitterion vor, dessen Bildung dadurch zu erklären ist, dass das Proton der Carboxygruppe zum Guanidino-Rest wandert, der stärker basisch als die α-Aminogruppe ist:[5]
Im elektrischen Feld wandert das Zwitterion nicht, da es als Ganzes ungeladen ist. Genaugenommen ist dies am isoelektrischen Punkt (bei einem bestimmten pH-Wert, hier 11,2[6]) der Fall, bei dem das Arginin auch seine geringste Löslichkeit in Wasser besitzt.
Freies L-Arginin hat einen bitteren Geschmack.[7]
Stereochemie
In den Proteinen kommt ausschließlich L-Arginin [Synonym: (S)-Arginin] peptidisch gebunden vor. Enantiomer dazu ist das spiegelbildliche D-Arginin [Synonym: (R)-Arginin], das in Proteinen nicht vorkommt. Racemisches DL-Arginin [Synonym: (RS)-Arginin] besitzt geringe Bedeutung.
Biosynthese
Im Harnstoffzyklus entsteht L-Arginin aus Carbamoylphosphat, L-Ornithin und L-Aspartat.
Funktionen
L-Arginin ist eine Quelle energiereicher Stickstoff-Phosphat-Verbindungen in Organismen und ist an zahlreichen biologischen Funktionen beteiligt. Es dient in Keimlingen und Speicherzellen als Stickstoff-Reservoir. L-Arginin ist ein Metabolit des Harnstoffzyklus, in dem der Ammoniak, der beim Abbau von Stickstoffverbindungen (z. B. Aminosäuren) entsteht, in Harnstoff umgewandelt wird. L-Arginin ist die alleinige Vorstufe von Stickstoffmonoxid (NO), einem der kleinsten Botenstoffe im menschlichen Körper. Durch Stickstoffmonoxid (NO)-Synthase entsteht aus L-Arginin der Endothelium-derived relaxing Factor (EDRF), der als NO identifiziert wurde. EDRF führt physiologisch zu einer Gefäßerweiterung, indem das NO in die Muskelschicht der Gefäße diffundiert. Es aktiviert dort die lösliche Guanylatcyclase und führt so zur Erschlaffung der glatten Muskulatur und zum Nachlassen des Gefäßtonus. Aufgrund der gefäßerweiternden Funktion findet Arginin im Bodybuilding als sogenanntes „Pump-Supplement“ Anwendung, ohne dass diese biologische Wirkung bewiesen ist. Weiterhin führt das NO zur Hemmung der Thrombozytenaggregation und -adhäsion. Dadurch wird die Bereitschaft für thrombotische Veränderungen an Gefäßplaque-Rupturen herabgesetzt, dem häufigsten Grund für cerebrale Insulte. Es wird angenommen, dass Arginin die unterdrückte Immunantwort bei schweren Verletzungen, Mangelernährung, Sepsis und nach Operationen positiv beeinflussen kann. Bei zusätzlicher Gabe wird eine verbesserte zelluläre Immunantwort, eine Abnahme verletzungsbedingter Funktionsstörungen der T-Zellen und eine verstärkte Phagozytose beobachtet. Zusätzlich wird die Ausbildung der endothelialen Dysfunktion (gestörten Gefäßfunktion) verhindert.[8][9]
1998 erhielten die Wissenschaftler Robert F. Furchgott, Louis J. Ignarro und Ferid Murad für die Erforschung des Zusammenhangs von Arginin und NO den Nobelpreis für Medizin.
Bedarf
Der Mensch kann innerhalb des Harnstoffzyklus Arginin selbst synthetisieren, allerdings sind die entstehenden Mengen nicht ausreichend, um den Bedarf vor allem bei heranwachsenden Menschen vollständig zu decken. Daher ist L-Arginin für Kinder essentiell. Aber auch bei Erwachsenen wird der Bedarf an L-Arginin durch die körpereigene Produktion oft nicht ausreichend abgedeckt. Besonders in der Wachstumsphase, durch Stress, bei diversen Krankheiten (z. B. Arteriosklerose, Bluthochdruck, erektile Dysfunktion, Gefäßerkrankungen) oder nach Unfällen übersteigt der Bedarf an Arginin die vom menschlichen Organismus produzierte Menge. Arginin wird daher heute zu den essentiellen Aminosäuren gezählt.
Bei einer Proteinzufuhr von etwa 70–90 g/Tag ergibt sich eine rechnerische tägliche Argininzufuhr von ca. 2–5 g/Tag.[10]
Medizinische Verwendung
L-Arginin-Hydrochlorid wird zur Behandlung einer schweren metabolischen Alkalose verwendet. In der Kinderheilkunde ist L-Arginin-Hydrochlorid auch zur Behandlung eines durch eine schwere angeborene Stoffwechselstörung bedingten erhöhten Ammoniakgehaltes im Blut (Hyperammonämie) angezeigt. Diagnostisch wird L-Arginin-Hydrochlorid zur Abklärung eines Wachstumshormonmangels bei Minderwuchs eingesetzt.
Als (semi)essentielle Aminosäure ist L-Arginin obligatorischer Bestandteil einer parenteralen Ernährung. In Elektrolyt-Konzentraten (Zusatz als Hydrochlorid zu Infusionslösungen) und in peroralen Diätetika wird L-Arginin ebenfalls eingesetzt.[11]
Supplemente
Arginin wird auch als Nahrungsergänzungsmittel, diätetisches Lebensmittel für Sportler oder ergänzend bilanzierte Diät angeboten.[12]
Als diätetisches Lebensmittel für Sportler "mit intensiven Muskelanstrengungen".
Als ergänzend bilanzierte Diät mit folgenden Zweckbestimmungen (typische Beispiele):
- "zur diätetischen Behandlung von Atherosklerose, endothelialer Dysfunktion und zur Unterstützung des Kreislaufsystems."
- "zur diätetischen Behandlung der erektilen Dysfunktion."
Bei der Herz-Kreislauf-Zweckbestimmung sind oft andere Mikronährstoffe (Homocysteinsenker) zugefügt.
Die diätetische orale Argininzufuhr ist zur Zeit mangels randomisierter klinischer Studien mit harten Endpunkten (Herzinfarkt, Tod durch Herz-Kreislauf-Erkrankung) nicht als praktische Therapieoption zu sehen.[13] Die Studien wurden mit Surrogatmarkern (Fluss-vermittelte Dilatation, Unterarmblutfluss) durchgeführt und zeigten heterogene – mehrfach positive, aber auch negative – Effekte.
Die Zweckbestimmung "erektile Dysfunktion" beruht im Wesentlichen auf zwei Studien:[14][15] Ein positiver Effekt konnte (trotz Verblindung) nur bei subjektiven Parametern gefunden werden, auf objektive Parameter (wie Standard-Fragebögen oder Blutfluß-Parameter) zeigte sich kein Effekt. Eine Studie mit negativem Ausgang – allerdings mit einer niedrigen Dosierung von 1,5 g – liegt ebenfalls vor.[16] Gleichwohl zielt die evidenz-bewiesene Therapie der erektilen Dysfunktion mit PDE-5-Hemmern wie Sildenafil ("Viagra") darauf, den Abbau des direkten Stoffwechselproduktes des L-Arginins, dem NO, zu blockieren und so dessen Wirkung/Präsenz zu erhöhen und prolongieren. Es muss also die Frage beantwortet werden, welche orale Dosis überhaupt einen Konzentrationsanstieg im Zielgewebe verursachen kann.
Zufuhrmengen:
- In ergänzend bilanzierten Diäten sind durchschnittlich ca. 1,5 bis max. 6 g täglich enthalten.
- Nahrungsergänzungsmittel weisen oft deutlich geringere Zufuhrmengen von ca. 0,5 g täglich auf, deren physiologische Wirkung bei den oben genannten Zufuhrmengen irrelevant sein dürfte.
Einzelnachweise
- ↑ a b c d e f Datenblatt Arginin bei Carl Roth, abgerufen am 13. März 2010.
- ↑ a b c Teresa, K.-J. et al.: Nickel Ion Complexes of Amino Acids and Peptides. In: Metal Ions in Life Sciences Band 2: Nickel and Its Surprising Impact in Nature; John Wiley & Sons 2007; ISBN 978-0-470-01671-8; S. 67; doi:10.1002/9780470028131.ch3.
- ↑ a b Eintrag zu CAS-Nr. 74-79-3 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. März 2011 (JavaScript erforderlich)
- ↑ Nährstoffdatenbank des US-Landwirtschaftsministeriums, 22. Ausgabe.
- ↑ Hans-Dieter Jakubke und Hans Jeschkeit: Aminosäuren, Peptide, Proteine, Verlag Chemie, 1982, S. 42, ISBN 3-527-25892-2.
- ↑ Norman L. Allinger, Michael P. Cava, Don C. de Jongh, Carl R. Johnson, Norman A. Lebel und Calvin L. Stevens: Organische Chemie, Verlag Walther de Gruyter, 1980, S. 1129, ISBN 3-11-004594-X.
- ↑ W. Ternes, A. Täufel, L. Tunger, M. Zobel (Hrsg.): Lebensmittel-Lexikon. 4. Auflage, Behr’s Verlag, Hamburg 2005; S. 62–63; ISBN 3-89947-165-2.
- ↑ Landmesser, U. et al. (2004): Endothelial function: a critical determinant in atherosclerosis? In: Circulation, 109 (21 Suppl 1); II27–33; PMID 15173060; PDF (freier Volltextzugriff, engl.).
- ↑ P. Fürst, H-K. Biesalki et. al.: Ernährungsmedizin, S. 94–95, Thieme-Verlag, Stuttgart 2004.
- ↑ Hahn, Andreas: Nahrungsergänzungsmittel und ergänzende bilanzierte Diäten. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH Stuttgart, 2006; S. 295.
- ↑ S. Ebel und H. J. Roth (Herausgeber): Lexikon der Pharmazie, Georg Thieme Verlag, 1987, S. 56, ISBN 3-13-672201-9.
- ↑ Frank Jester: Arginin, der natürliche Kraftstoff für Blut, Kreislauf und Gesundheit, ISBN 978-3-00-031619-7, www.argininbuch.de.
- ↑ Bode-Böger: Einfluss von L-Arginin auf die Aterioskleroseentwicklung. In: Dtsch Med Wochenschr 2006; 130: S. 593–598.
- ↑ Chen J, Wollman Y, Chernichovsky T, Iaina A, Sofer M, Matzkin H: Effect of oral administration of high-dose nitric oxide donor L-arginine in men with organic erectile dysfunction: results of a double-blind, randomized, placebo-controlled study. In: BJU Int. 1999 Feb;83(3):269-73.
- ↑ Zorgniotti AW, Lizza,EF: Effect of large dose of the nitric oxide precursor L-arginine, on erectile dysfunction In: Int. J. Impot. Res. 1994; 6: 333-5.
- ↑ Klotz T, Mathers MJ, Braun M, Bloch W, Engelmann U.: Effectiveness of oral L-arginine in first-line treatment of erectile dysfunction in a controlled crossover study In: Urol Int. 1999;63(4):220-3.
Weblinks
 Wiktionary: Arginin – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Arginin – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen Proteinogene Aminosäuren
Proteinogene AminosäurenAlanin | Arginin | Asparagin | Asparaginsäure | Cystein | Glutamin | Glutaminsäure | Glycin | Histidin | Hydroxylysin | Isoleucin | Leucin | Lysin | Methionin | Phenylalanin | Prolin | Pyrrolysin | Selenocystein | Selenomethionin | Serin | Threonin | Tryptophan | Tyrosin | Valin
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Arginin — Arginin, Abk. Arg, Proteinbaustein, basische Aminosäure, die im Harnstoffzyklus Vorstufe des Harnstoffs ist … Deutsch wörterbuch der biologie
arginin — argìnīn m <G arginína> DEFINICIJA kem. C6H14N4O2, aminokiselina od ključne važnosti za razvoj djece; produkt je hidrolize mnogih bjelančevina … Hrvatski jezični portal
Arginin — Ar|gi|nin 〈n. 11; chem. 〉 essenzielle Aminosäure * * * Ar|gi|nin [zu ↑ Argentum (Silber bildet schwerlösliche A. Salze); ↑ in (3)], das; s, e; Symbol: Arg, R; Syn.: 2 Amino 5 guanidinovaleriansäure: H2N C(=NH) NH (CH2)3 CH(NH2) COOH; in… … Universal-Lexikon
Arginin-Vasopressin — Vasopressin; Adiuretin Kalottenmodell … Deutsch Wikipedia
Arginin — Argini̱n [wohl zu gr. ἀργινοεις = weiß, hell schimmernd] s; s, e: für den Stoffwechsel wichtige Aminosäure (Zwischenstufe beim Abbau der Proteine zu Harnstoff) … Das Wörterbuch medizinischer Fachausdrücke
Arginin — Ar|gi|nin das; s, e <zu gr. arginóeis »hell schimmernd« u. ↑...in> lebenswichtige ↑Aminosäure, die in allen Eiweißkörpern enthalten ist … Das große Fremdwörterbuch
Arginin-Vasopressin — AVP; Antidiuretisches Hormon; Vasopressin; Adiuretin; ADH … Universal-Lexikon
L-Arginin — Strukturformel L Arginin (oben) bzw. D … Deutsch Wikipedia
Twin Arginin Translocation — Als Twin Arginine Translocation (engl. für Twin Arginin Transport), kurz Tat, auch Tat System, wird in der Biochemie ein spezielles Transportsystem für Proteine in Pflanzen, Bakterien und Archaeen bezeichnet. Dieser Proteintransportweg wird in… … Deutsch Wikipedia
Endotheliale Stickstoffmonoxid-Synthase — Masse/Länge Primärstruktur 1202 Aminosäuren … Deutsch Wikipedia