- Kaliumhypochlorit
-
Strukturformel 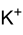
Allgemeines Name Kaliumhypochlorit Andere Namen Javelwasser (wässrige Lösung)
Summenformel KClO CAS-Nummer 7778-66-7 PubChem 23665762 Kurzbeschreibung nur in wässriger Lösung beständig[1]
Eigenschaften Molare Masse 90,55 g·mol−1 Löslichkeit mischbar mit Wasser[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] keine Einstufung verfügbar H- und P-Sätze H: siehe oben EUH: siehe oben P: siehe oben EU-Gefahrstoffkennzeichnung für KClO-Lösung[1] 
Ätzend (C) R- und S-Sätze R: 31-34 S: (1/2)-28-45-50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Kaliumhypochlorit (KClO) ist das Kaliumsalz der Hypochlorigen Säure (Unterchlorige Säure).
Inhaltsverzeichnis
Gewinnung und Darstellung
Es wird durch Einleiten von Chlorgas in Kalilauge oder durch Elektrolyse einer Kaliumchlorid-Lösung hergestellt.
Bei Abkühlen der konzentrierten Lösung auf -10 °C scheidet sich kristallines Hydrat ab, welches sehr reaktionfähig ist und brandfördernd wirkt.
Eigenschaften
Kaliumhypochlorit ist nur in wässriger Lösung haltbar und besitzt in dieser Form eine gelbgrüne Färbung. Die wässrige Lösung reagiert stark alkalisch. Beim Erhitzen zersetzt sich die Verbindung, wobei Chlorverbindungen wie Chlorwasserstoff frei werden.
Verwendung
Verdünnte Lösungen werden als Eau de Javel (Javelwasser) verkauft. Diese werden zum Bleichen, Oxidieren oder, wegen seiner antimikrobiellen Wirkung, zum Desinfizieren verwendet. Ferner findet es Verwendung bei der Entgiftung cyanidhaltiger Abwässer.
Einzelnachweise
- ↑ a b c Eintrag zu Kaliumhypochlorit-Lösung mit aktivem Chlor in der GESTIS-Stoffdatenbank des IFA, abgerufen am 7. Februar 2008 (JavaScript erforderlich)
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
Kategorien:- Ätzender Stoff
- Kaliumverbindung
- Hypochlorit
Wikimedia Foundation.

