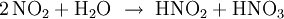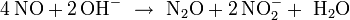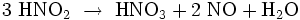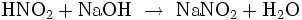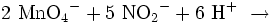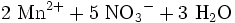- HNO2
-
Strukturformel 
Allgemeines Name Salpetrige Säure Andere Namen - Hydrogennitrit
- Stickstoff(III)-säure
Summenformel HNO2 CAS-Nummer 7727-54-0 Eigenschaften Molare Masse 47,01 g/mol pKs-Wert 3,29 [1]
Sicherheitshinweise Gefahrstoffkennzeichnung 
unbekannt R- und S-Sätze R: ? S: ? Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Salpetrige Säure (nach der Nomenklatur der IUPAC Hydrogennitrit genannt) ist eine nur in kalter, verdünnter, wässriger Lösung beständige, schwache Säure.
Inhaltsverzeichnis
Synthese
Beim Einleiten in Wasser, z. B. im Rahmen des Ostwald-Verfahrens, disproportioniert Stickstoffdioxid NO2 in Salpetersäure und Salpetrige Säure:
Daher kann NO2 formal als gemischtes Anhydrid von HNO2 und HNO3 betrachtet werden. In ähnlicher Weise lassen sich die Salze der Salpetrigen Säure, die Nitrite mit dem Anion NO2-, durch Disproportionierung von Stickstoffmonoxid NO in konzentrierten Laugen bei hohen Temperaturen herstellen[1]:
Als Zwischenprodukt entsteht hierbei Hyponitrit N2O22-, das bei den Reaktionsbedingungen instabil ist und unter Freisetzung von Distickstoffmonoxid zerfällt.
Reaktionsverhalten
Salpetrige Säure zerfällt bei Erwärmung zu Salpetersäure und Stickstoffmonoxid:
Versetzt man Salpetrige Säure mit alkalischen Lösungen, bilden sich die stabileren Nitrite. Beispielsweise entsteht bei der Reaktion von Salpetriger Säure mit verdünnter Natronlauge Natriumnitrit:
Da das Stickstoff-Atom in der Salpetrigen Säure die Oxidationsstufe +III besitzt, kann Salpetrige Säure durch starke Oxidationsmittel zu Salpetersäure oxidiert werden (Oxidationsstufe +V). So gelingt eine Oxidation der salpetrigen Säure mit schwefelsaurer Kaliumpermanganat-Lösung:
Nachweis
Eine einfache, aber nicht spezifische Nachweismethode ist die Oxidation von Iodid zu Iod durch Salpetrige Säure. Man bedient sich hierbei der Iod-Stärke-Reaktion, die schon sehr geringe Konzentrationen (wenige ppm) Salpetriger Säure durch den entstandenen Polyiodid-Stärke-Komplex mittels Blaufärbung anzeigt. Hierzu wird das sog. Kaliumiodidstärkepapier benutzt.
Spezifisch können Salpetrige Säure bzw. Nitrite mit Lunges Reagenz nachgewiesen werden, wobei sich ein roter Azofarbstoff bildet.
Toxizität
Salpetrige Säure ist ein Mutagen und hat eine negative Wirkung auf Organismen. Die Säure kann Cytosin in Uracil umwandeln. Da Uracil aber komplementär zu Adenin ist, entsteht eine Punktmutation.
Siehe auch
- Salpetersäure HNO3 (Hydrogennitrat)
Einzelnachweise
Wikimedia Foundation.