- Gibbssche Phasenregel
-
Die Gibbssche Phasenregel (nach Josiah Willard Gibbs 1876) beinhaltet die Aussage, dass im thermodynamischen Gleichgewicht nicht beliebig viele Phasen gleichzeitig nebeneinander vorliegen können. Zudem kann man mit ihr die an einem bestimmten Punkt im Phasendiagramm maximal möglichen Freiheitsgrade bestimmen. Für ein physikalisch homogenes thermodynamisches System reichen zwei Zustandsgrößen zur Bestimmung des Gleichgewichtszustands aus.
Die Herleitung der Gibbsschen Phasenregel erfolgt über die Gibbs-Duhem-Gleichung, die zeigt, dass in einem thermodynamischen System nicht alle intensiven Variablen unabhängig voneinander veränderlich sind.
Inhaltsverzeichnis
Phasenregel für Gase und Flüssigkeiten
Für Fluide, also Gase und Flüssigkeiten, lautet sie:
- N - Anzahl der unabhängigen Komponenten im System (z. B. H2O, CO2)
- P - Anzahl der Phasen (verschiedene Aggregatzustände einer oder mehrerer Komponenten oder koexistierende flüssige Phasen (z. B. sind Wasser und Öl nicht mischbar und bilden zwei Phasen))
- f - Anzahl der Freiheitsgrade (hier: Anzahl der Zustandsvariablen die geändert werden können, ohne dass sich die Zahl der Phasen des Systems ändert)
Die Anzahl der existierenden Phasen in Abhängigkeit von N und f wird in der folgenden Tabelle dargestellt:
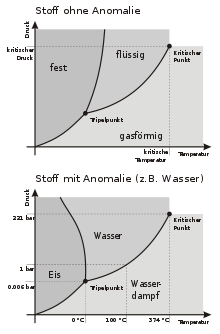
N=1 N=2 N=3 f=0 3 4 5 f=1 2 3 4 f=2 1 2 3 f=3 1 2 Daraus folgt zum Beispiel für ein einkomponentiges System (N = 1), welches in zwei verschiedenen Aggregatzuständen (P = 2) vorliegt, dass es genau einen verbleibenden Freiheitsgrad gibt, das heißt eine Koexistenzlinie im Phasendiagramm. Existieren gleichzeitig drei Phasen (z. B. Wasser flüssig, gasförmig und fest), so verbleibt genau ein Punkt im Phasendiagramm, der Tripelpunkt, da kein Freiheitsgrad verbleibt (f=0).
Weiterhin folgt, dass es in einem einkomponentigen System an einer Stelle maximal drei koexistierende Phasen geben kann, da
 (siehe Tripelpunkt in Graphik rechts); in einem zweikomponentigen vier Phasen, usw..
(siehe Tripelpunkt in Graphik rechts); in einem zweikomponentigen vier Phasen, usw..Phasenregel für Feststoffe
Da bei Feststoffen eine (geringe) Änderung des Druckes auf Grund des geringen Gasdrucks keine beziehungsweise nur sehr geringe Auswirkungen hat, lautet die Gibbssche Phasenregel in diesem Fall:
Diese Vereinfachung gilt jedoch nicht bei höheren Drücken, wie sie beispielsweise bereits in der Erdkruste vorliegen. Für die Druck- und Temperaturermittlung in der Geothermobarometrie ist dies für die korrekte Erfassung der jeweiligen Gleichgewichts-Paragenese von großer Bedeutung.
Siehe auch
Weblinks
Mogk, David: Teaching Phase Equilibria. Gibbs' Phase Rule: Where it all Begins (Die Phasenregel in der Geologie)
Wikimedia Foundation.