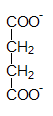- E363
-
Strukturformel 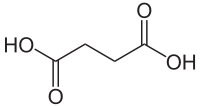
Allgemeines Name Bernsteinsäure Andere Namen - Butandisäure
- Succinylsäure
Summenformel C4H6O4 CAS-Nummer 110-15-6 PubChem 1110 Kurzbeschreibung farb- und geruchloser kristalliner Feststoff [1] Eigenschaften Molare Masse 118,09 g·mol−1 Aggregatzustand fest
Dichte 1,55 g·cm−3 [1]
Schmelzpunkt 184 °C [1]
Siedepunkt 235 °C [1]
Löslichkeit löslich in Wasser: 58 g·l−1 (20 °C) [1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Reizend (Xi) R- und S-Sätze R: 36 S: 26 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Bernsteinsäure, auch Succinylsäure oder Butandisäure, E 363, ist eine farblose, kristalline aliphatische Dicarbonsäure. Die Kristalle sind in siedendem Wasser gut löslich.
Inhaltsverzeichnis
Vorkommen und Herstellung
Im Stoffwechsel aller Organismen kommt das Salz der Bernsteinsäure beim Abbau von Glucose als Zwischenstufe bei der Regeneration des Akzeptors Oxalessigsäure vor. Es ist entsprechend ein Stoffwechsel-Zwischenprodukt des Citratcyclus, außerdem kommt sie im Harnstoffzyklus vor. In der Natur kommt Bernsteinsäure zudem in vielen Pflanzensäften sowie in Algen und Pilzen vor.[2]
Die technische Synthese von Bernsteinsäure erfolgt über eine Hydrierung der Maleinsäure, die Oxidation von 1,4-Butandiol (BDO) oder die Oxo-Synthese von Acethylen.[3]
Bernsteinsäure kann auch durch Fermentation aus nachwachsenden Rohstoffen hergestellt werden, insbesondere aus Stärke und verschiedenen Oligosacchariden (C6- und C5-Zucker).[4] Hierbei kann das natürliche Vorkommen der Bernsteinsäure im Stoffwechsel genutzt werden, um sie gezielt durch Mikroorganismen herstellen zu lassen. Dieser Syntheseweg kann bislang allerdings aus Kostengründen noch nicht mit der Maleinsäuresynthese konkurrieren und ist teilweise noch nicht vollständig für den großtechnischen Einsatz ausgereift.
Als Succinate bezeichnet man die Salze und Ester der Bernsteinsäure. Der Begriff 'Succinat' leitet sich vom lateinischen Wort suc(c)inum für Bernstein ab. Sie enthalten in ihren Kristallgittern das Succinat-Ion als negativ geladenes Anion. Die allgemeine Formel eines Alkalisuccinats lautet MOOC–CH2–CH2–COOM, M steht besonders für Natrium- und Kaliumionen. Alkalisuccinate lösen sich leicht in Wasser. Die Erdalkalisuccinate sind nur schwer, die übrigen Succinate gar nicht wasserlöslich. So findet man Calciumsuccinat in unreifen Früchten oder Algen. Die esterartigen Succinate können durch die Halbstrukturformel R–O–CO–CH2–CH2–CO–O–R beschrieben werden.
Wird Bernsteinsäure erhitzt, spaltet sie Wasser ab und bildet unter Ringschluß das Bernsteinsäureanhydrid.[2]
Verwendung
Verwendung im Lebensmittelbereich
Bernsteinsäure ist in der EU als Lebensmittelzusatzstoff der Nummer E 363 zugelassen und dient aufgrund des mild sauren und zugleich leicht salzigen Geschmacks als Geschmacksverstärker für Desserts, Trockensuppen und Getränkepulver. Als Kochsalzersatz in Diätkost werden verschiedene Salze der Bernsteinsäure genutzt (Fe, Mg, Ca, K).[3] Aufgrund der körpereigenen Produktion und Verstoffwechslung von Bernsteinsäure, die beim Menschen etwa 1 kg pro Tag beträgt, wird Bernsteinsäure als unbedenklich angesehen.[2]
Während der alkoholischen Gärung sowie beim späteren Ausbau des Weins in Gebinden wie dem Holzfass oder dem Edelstahlbehälter entstehen neben den zentralen Säuren des Weins (Weinsäure, Äpfelsäure und Citronensäure) auch Bernsteinsäure sowie Essigsäure, Buttersäure und Milchsäure. Bernsteinsäure entsteht dabei vor allem bei der Kohlensäuremaischung und schmeckt leicht bitter und salzig, die Veresterung Monomethylsuccinat bringt eine mild-fruchtige Komponente in den Wein.
Technische Verwendungen
Bernsteinsäure wird zur Herstellung von Farbstoffen und Lacken sowie als Harz zur Herstellung von Polyester- und Alkydharzen verwendet.[3] Einige mit Polyalkoholen veresterte Succinate verwendet man als Lösemittel und Weichmacher für Kunststoffe und Wachse, weitere Ester finden Verwendung in der Parfumherstellung. In Form von Sulfobernsteinsäureestern wird Bernsteinsäure auch als wichtige Tensidgruppe verwendet, diese werden jedoch in der Regel auf der Basis von Maleinsäure hergestellt.
Bernsteinsäure ist zudem einer der zentralen Hoffnungsträger für die Industrielle Biotechnologie als Rohstoff für verschiedene Plattformchemikalien und Polymere. Wie dargestellt kann Bernsteinsäure durch Fermentation aus Stärke hergestellt werden. Die Bernsteinsäure selbst kann als Ausgangsstoff für die biotechnologische Produktion einer Reihe von Plattform- und Spezialchemikalien dienen, darunter 1,4-Butandiol (BDO), 1,4-Butandiamin, Tetrahydrofuran (THF), N-Methyl-2-pyrrolidon (NMP), γ-Butyrolactam, Butyro-1,4-lacton (GBL) und einige weitere.[4]
Geschichte
Die Bernsteinsäure wurde 1546 von Georgius Agricola bei der trockenen Destillation durch Erhitzen von Bernstein entdeckt.
Belege
Zitierte Belege
- ↑ a b c d e f Eintrag zu CAS-Nr. 110-15-6 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 9. August 2007 (JavaScript erforderlich)
- ↑ a b c Artikel Bernsteinsäure in Brockhaus Enzyklopädie online, Bibliographisches Institut & F. A. Brockhaus AG 2005 - 2009.
- ↑ a b c Stichwort Succinic Acid In: Hans Zoebelein (Hrsg.): Dictionary of Renewable Ressources. 2. Auflage, Wiley-VCH, Weinheim und New York 1996; Seite 92. ISBN 3-527-30114-3.
- ↑ a b Werpy et al. 2006
Literatur
- Todd Werpy, John Frye, John Holladay: Succinic Acid - A Model Building Block for Chemical Production from Renewable Resources. In: Birgit Kamm, Patrisk R. Gruber, Michael Kamm (Hrsg.): Biorefineries - Industrial Processes and Products. Status Quo and Future Directions. Vol. 2. Wiley-VCH Verlag, Weinheim 2006; S. 367-379. ISBN 3-527-31027-4.
Weblinks
Wikimedia Foundation.