- DNA-Sequenzierung
-
DNA-Sequenzierung ist die Bestimmung der Nukleotid-Abfolge in einem DNA-Molekül. Die DNA-Sequenzierung hat die biologischen Wissenschaften revolutioniert und die Ära der Genomik eingeleitet. Seit 1995 konnte durch DNA-Sequenzierung das Genom von über 1000 (Stand: 2010) verschiedenen Organismen analysiert werden (siehe Sequenzierte Organismen). Zusammen mit anderen DNA-analytischen Verfahren wird die DNA-Sequenzierung u. a. auch zur Untersuchung genetisch bedingter Erkrankungen herangezogen. Darüber hinaus ist die DNA-Sequenzierung als analytische Schlüsselmethode, insbesondere im Rahmen von DNA-Klonierungen (engl. molecular cloning), aus einem molekularbiologischen bzw. gentechnischen Laborbetrieb, heute nicht mehr wegzudenken.
Inhaltsverzeichnis
Problemstellung
Die DNA-Sequenzierung als Ablesen der Nukleotidfolge von DNA war über Jahrzehnte hinweg bis in die Mitte der siebziger Jahre ein ungelöstes Problem, bis entsprechende biochemische bzw. biotechnologische Methoden entwickelt wurden. Heutzutage ist selbst die Sequenzierung ganzer Genome vergleichsweise schnell und einfach geworden[1]. Die Herausforderung beschränkt sich jedoch nicht nur auf das direkte Ablesen der Nukleotidsequenz. Je nach Verfahren werden in jeder einzelnen Sequenzierreaktion auf Grund technischer Beschränkungen nur kurze DNA-Abschnitte (engl. reads) bis maximal 1000 Basenpaare abgelesen. Ein größeres Sequenzierprojekt, wie das Humangenomprojekt, bei dem mehrere Milliarden Basenpaare sequenziert wurden, erfordert darum eine Herangehensweise, die als Shotgun Sequencing bezeichnet wird. Dabei werden längere DNA-Abschnitte zunächst in kleinere Einheiten zerlegt, diese dann sequenziert und die Sequenzinformationen der einzelnen kurzen Abschnitte anschließend mit bioinformatischen Methoden wieder zu einer vollständigen Gesamtsequenz zusammengefügt. Um aus den rohen Sequenzdaten biologisch relevante Informationen zu gewinnen (beispielsweise Informationen über vorhandene Gene und deren Kontrollelemente), schließt sich an die Sequenzierung die DNA-Sequenzanalyse an. Ohne sie bleibt jede Sequenzinformation ohne wissenschaftlichen Wert.
Sequenzierungsmethoden
Es gibt heute mehrere Verfahren zum Ablesen der Sequenzinformation von einem DNA-Molekül. Lange Zeit waren überwiegend Weiterentwicklungen der Methode nach Frederick Sanger in Verwendung. Moderne Verfahren bieten Möglichkeiten der beschleunigten Sequenzierung durch hochparallelen Einsatz. Die nach der Sanger-Methode entwickelten Sequenzierungsverfahren werden häufig als Sequenzierung der nächsten Generation (engl. next generation sequencing) bezeichnet.
Klassische Methoden
Methode von Maxam und Gilbert
Die Methode von Allan Maxam und Walter Gilbert von 1977 beruht auf der basenspezifischen chemischen Spaltung der DNA durch geeignete Reagenzien und anschließender Auftrennung der Fragmente durch Gelelektrophorese.[2] Die DNA wird zunächst am 5' oder 3'-Ende mit radioaktivem Phosphat oder nicht-radioaktiv (Biotin, Fluorescein) markiert. In vier getrennten Ansätzen werden dann jeweils bestimmte Basen vom Zucker-Phosphat-Rückgrat der DNA modifiziert und abgespalten, beispielsweise wird die Base Guanin (G) durch das Reagenz Dimethylsulfat methyliert und durch Alkalibehandlung mit Piperidin entfernt. Danach wird der DNA-Strang an den jetzt basenlosen Stellen komplett gespalten. In jedem Ansatz entstehen Fragmente unterschiedlicher Länge, deren 3'-Ende stets an bestimmten Basen gespalten worden war. Die Gelelektrophorese trennt die Fragmente nach der Länge auf, wobei Längenunterschiede von einer Base aufgelöst werden. Durch Vergleich der vier Ansätze auf dem Gel lässt sich die Sequenz der DNA ablesen. Ihren Erfindern ermöglichte diese Methode die Bestimmung der Operon-Sequenz eines Bakteriengenoms. Die Methode kommt heute kaum noch zum Einsatz, da sie gefährliche Reagenzien benötigt und schwerer automatisierbar ist als die zur gleichen Zeit entwickelte Didesoxymethode nach Sanger.
Didesoxymethode nach Sanger
Die Didesoxymethode nach Sanger wird auch Kettenabbruch-Synthese genannt und stellt eine enzymatische Methode dar. Sie wurde von Sanger und Coulson um 1975 entwickelt und bereits 1977 mit der ersten vollständigen Sequenzierung eines Genoms (Bakteriophage φX174 [3]) vorgestellt.[4] Sanger erhielt für seine Arbeiten zur DNA-Sequenzierung zusammen mit Walter Gilbert und Paul Berg 1980 den Nobelpreis für Chemie.[5]
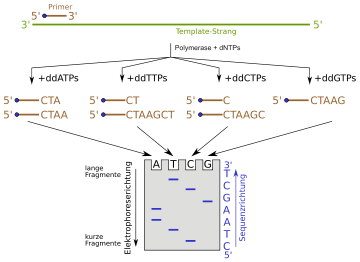 Prinzip der DNA-Sequenzierung nach der Didesoxy-Methode.
Prinzip der DNA-Sequenzierung nach der Didesoxy-Methode.
dNTP ist die allgemeine Abkürzung für ein Nukleosidtriphosphat und kann für dATP, dCTP, dGTP oder dTTP stehen. ddNTPs sind die entsprechenden Didesoxy-Varianten der dNTPs. Der Einbau eines ddNTPs führt zum Abbruch der Polymerisationsreaktion. Die blauen Punkte am 5'-Ende des Primers stellen eine Markierung dar (z. B. eine fluoreszierende Gruppe), mittels der die Syntheseprodukte später im Gel sichtbar gemacht werden können. Alternativ lassen sich auch radioaktiv markierte Nukleosidtriphosphate zur Polymerisationsreaktion einsetzen.Ausgehend von einem kurzen Abschnitt bekannter Sequenz (Primer) wird durch eine DNA-Polymerase einer der beiden komplementären DNA-Stränge verlängert. Zunächst wird die DNA-Doppelhelix durch Erwärmung denaturiert, woraufhin Einzelstränge für das weitere Vorgehen zur Verfügung stehen. In vier sonst gleichen Ansätzen (alle beinhalten die vier Nukleotide) wird je eine der vier Basen zum Teil als Didesoxynukleosidtriphosphat (ddNTP) zugegeben (also je ein Ansatz mit entweder ddATP, ddCTP, ddGTP oder ddTTP). Diese Kettenabbruch-ddNTPs besitzen keine 3'-Hydroxygruppe: Werden sie in den neusynthetisierten Strang eingebaut, ist eine Verlängerung der DNA durch die DNA-Polymerase nicht mehr möglich, da die OH-Gruppe am 3'-C-Atom für die Verknüpfung mit der Phosphatgruppe des nächsten Nukleotids fehlt. In der Folge entstehen DNA-Fragmente unterschiedlicher Länge, die in jedem Ansatz stets mit dem gleichen ddNTP enden (also nur mit A oder C oder G oder T). Entweder der Primer oder die ddNTPs sind radioaktiv markiert. Nach der Sequenzier-Reaktion werden die markierten Abbruchprodukte aus jedem Ansatz mittels Polyacrylamid-Gelelektrophorese der Länge nach aufgetrennt. Durch Vergleich der vier Ansätze kann man die Sequenz nach der Entwicklung des radioaktiven Gels auf einem fotografischen Film ablesen. Die dementsprechend komplementäre Sequenz ist die Sequenz der verwendeten einsträngigen DNA-Matrize. Als Sequenzier-Reaktion kommt heutzutage eine Variation der Polymerase-Kettenreaktion (PCR) zum Einsatz. Anders als bei der PCR wird nur ein Primer eingesetzt, sodass die DNA nur linear amplifiziert wird.
Seit Anfang der neunziger Jahre werden vor allem mit Fluoreszenz-Farbstoffen markierte Didesoxynukleosidtriphosphate eingesetzt. Jedes der vier ddNTPs wird mit einem unterschiedlichen Farbstoff gekoppelt. Diese Modifikation erlaubt es, alle vier ddNTPs in einem Reaktionsgefäß zuzugeben, eine Aufspaltung in getrennte Ansätze und der Umgang mit Radioisotopen entfällt. Die entstehenden Kettenabbruchprodukte werden mittels Kapillarelektrophorese aufgetrennt und mit Hilfe eines Lasers zur Fluoreszenz angeregt. Die ddNTPs am Ende jedes DNA-Fragmentes zeigen dadurch Fluoreszenz unterschiedlicher Farbe und können so von einem Detektor erkannt werden. Das Chromatogramm (die Abfolge der Farbsignale, die am Detektor erscheinen) gibt direkt die Sequenz der Basen des sequenzierten DNA-Stranges wieder.
Moderne Ansätze
Mit der zunehmenden Bedeutung der DNA-Sequenzierung in der Forschung und Diagnostik wurden Methoden entwickelt, die einen erhöhten Durchsatz erlauben. Damit ist es nun möglich, das komplette menschliche Genom in etwa 8 Tagen zu sequenzieren [6]. Die entsprechenden Verfahren werden als Sequenzierung der zweiten Generation (engl. second generation sequencing) bezeichnet. Verschiedene Firmen haben Verfahren mit unterschiedlichen Vor- und Nachteilen entwickelt. Außer den hier aufgeführten gibt es noch weitere.
Pyrosequenzierung
Die Pyrosequenzierung[7] nutzt wie die Sanger-Sequenzierung eine DNA-Polymerase, wobei der Typ der DNA-Polymerase durchaus noch unterschiedlich sein kann, zur Synthese des DNA-Gegenstranges. Allerdings wird die DNA-Polymerase gewissermaßen „in Aktion” beobachtet, wie sie nacheinander einzelne Nukleotide an einen neusynthetisierten DNA-Strang anhängt. Der erfolgreiche Einbau eines Nukleotids wird durch ein ausgeklügeltes Enzymsystem unter Beteiligung einer Luziferase in einen Lichtblitz umgesetzt und von einem Detektor erfasst. Die zu sequenzierende DNA dient als Matrizenstrang und liegt einzelsträngig vor. Ausgehend von einem Primer erfolgt die Strangverlängerung, Nukleotid um Nukleotid, durch Zugabe von jeweils einer der vier Arten Nukleosidtriphosphat (NTP). Bei Zugabe des passenden (komplementären) Nukleotids erhält man ein Signal, wurde ein an dieser Stelle nicht passendes NTP zugegeben, bleibt der Lichtblitz aus. Danach werden die vorhandenen NTP zerstört und eine andere Art wird zugesetzt, dies wird fortgesetzt bis sich wieder eine Reaktion zeigt (Spätestens nach der 4. Zugabe zeigt sich also eine Reaktion, da dann alle Arten NTP durchprobiert wurden). Bei Einbau eines komplementären Nukleotids durch die DNA-Polymerase wird Pyrophosphat (PPi) freigesetzt. Das Pyrophosphat wird durch die ATP-Sulfurylase zu Adenosintriphosphat (ATP) umgesetzt. Das ATP treibt die Luziferase-Reaktion an, wodurch Luziferin in Oxyluziferin umgesetzt wird. Dies resultiert wiederum in einem detektierbaren Lichtsignal – dessen Stärke proportional zum verbrauchten ATP ist.
Die Pyrosequenzierung wird beispielsweise zur Bestimmung der Häufigkeit von bestimmten Genmutationen (SNPs, engl. Single Nucleotide Polymorphism), z. B. bei der Untersuchung von Erbkrankheiten eingesetzt. Die Pyrosequenzierung ist gut automatisierbar und eignet sich zur hochparallelen Analyse von DNA-Proben.
Sequenzierung durch Hybridisierung
Zu diesem Zweck werden auf einem Glasträger (DNA-Chip oder Microarray) kurze DNA-Abschnitte (Oligonukleotide) in Reihen und Spalten fixiert. Die Fragmente der zu sequenzierenden DNA werden mit Farbstoffen markiert und das Fragmentgemisch wird auf der Oligonukleotidmatrix ausgebracht, so dass komplementäre fixierte und freie DNA-Abschnitte miteinander hybridisieren können. Nach dem Auswaschen ungebundener Fragmente lässt sich das Hybridisierungsmuster anhand der Farbmarkierungen und deren Stärke ablesen. Da die Sequenzen der fixierten Oligonukleotide und deren Überlappungsbereiche bekannt sind, kann man letztlich aus dem Farbmuster auf die zugrundeliegende Gesamtsequenz der unbekannten DNA rückschließen.
Einzelnachweise
- ↑ Pettersson E, Lundeberg J, Ahmadian A: Generations of sequencing technologies. In: Genomics. 93, Nr. 2, Februar 2009, S. 105–111. doi:10.1016/j.ygeno.2008.10.003. PMID 18992322.
- ↑ Maxam, A. & Gilbert, W. (1977): A new method of sequencing DNA. In: Proceedings of the National Academy of Sciences U.S.A. Bd. 74, S. 560–564; doi:10.1038/265687a0; PMID 265521; PMC 392330.
- ↑ Sanger F. et al. (1977): Nucleotide sequence of bacteriophage phi X174 DNA. In: Nature. Bd. 265, S. 687–695; PMID 870828.
- ↑ Sanger, F. et al. (1977): DNA sequencing with chain-terminating inhibitors. In: Proceedings of the National Academy of Sciences U.S.A. Bd. 74, S. 5463–5467; PMID 271968; PMC 431765.
- ↑ Informationen der Nobelstiftung zur Preisverleihung 1980 an Walter Gilbert, Paul Berg und Frederick Sanger (englisch)
- ↑ Genome sequencing: the third generation. 6. Februar 2009, abgerufen am 28. Februar 2011 (englisch).
- ↑ Ronaghi, M. (2001): Pyrosequencing sheds light on DNA sequencing. In: Genome Research. 11:3–11. PMID 11156611 doi:10.1101/gr.11.1.3 PDF
Literatur
- Laura Bonetta (2006): Genome sequencing in the fast lane. In: Nature Methods. Bd. 3, S. 141–147. doi:10.1038/nmeth0206-141 PDF
- Karin Hollricher: Hochleistungs-Sequenzieren. In: Laborjournal. Nr. 4, 2009, S. 44–48.
Hilfsmethoden
- Shotgun Sequencing
- Chromosome Walking
- Pyrosequencing
Weblinks
Kategorien:- Biologische Untersuchungsmethode
- DNA
Wikimedia Foundation.