- Tramadolhydrochlorid
-
Strukturformel 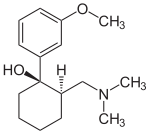
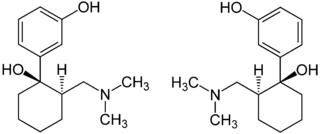
(1R,2R)-Tramadol (1S,2S)-Tramadol
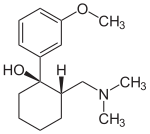
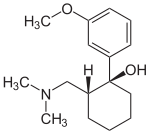
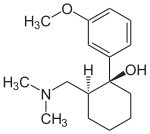
(1R,2S)-Tramadol (1S,2R)-TramadolAllgemeines Freiname Tramadol Andere Namen Summenformel C16H25NO2 CAS-Nummer - 27203-92-5 [Racemat aus (1R,2R)-Form und der (1S,2S)-Form]
- 36282-47-0 [Hydrochlorid, Racemat aus (1R,2R)-Form und der (1S,2S)-Form]
- 123134-25-8 [1S,2S)-Form]
- 148229-79-2 [Hydrochlorid, (1S,2S)-Form]
- 123154-38-1 [(1R,2R)-Form]
- 148229-78-1 [Hydrochlorid, (1R,2R)-Form]
- 152538-36-8 [Racemat aus (1R,2S)-Form und der (1S,2R)-Form]
- 73806-49-2 [Hydrochlorid, Racemat aus (1R,2S)-Form und der (1S,2R)-Form]
PubChem 33741 ATC-Code N02AX02
DrugBank DB00193 Arzneistoffangaben Wirkstoffklasse Fertigpräparate - Tramadol-Mepha® (CH)
- Tramadol-STADA ® (D)
- Tramal® (A)
Verschreibungspflichtig: Ja Eigenschaften Molare Masse 263,38 g·mol−1 Aggregatzustand Feststoff [1]
pKs-Wert 9,41 [1]
Löslichkeit löslich in Wasser (Hydrochloride)
Sicherheitshinweise Gefahrstoffkennzeichnung [2]
Xn
Gesundheits-
schädlichR- und S-Sätze R: 22 S: keine S-Sätze Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 WGK 2 (wassergefährdend) [2] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Tramadol ist ein mittelstark wirksames Opioid, welches zur Therapie mittelstarker Schmerzen eingesetzt wird. Der Wirkstoff wurde von dem Pharmaunternehmen Grünenthal als Racemat [1:1-Gemisch der (1R,2R)-Form und der (1S,2S)-Form] entwickelt. Off-Label wird es auch zur Behandlung vom Restless-Legs-Syndrom verwendet.
Tramadol ist in Deutschland u. a. als Tramal®, Tramadolor® von Hexal, Tramagit® und als Doloxene® im Handel. Es ist verschreibungspflichtig und unterliegt als eines von wenigen Opioiden nicht dem Betäubungsmittelgesetz.
Inhaltsverzeichnis
Wirkung
Tramadol ist ein reiner Agonist und neben Meptazinol (Handelsname Meptid®) das einzige injizierbare Opioid-Analgetikum, das nicht unter das BtMG fällt. Die analgetische Potenz beträgt das 0,1-fache von Morphin. Deshalb ist die Missbrauchsgefahr gering. Typischerweise enthält eine Ampulle 50 oder 100 mg Tramadol.
Bei Tramadol handelt es sich um einen nicht selektiven reinen Agonisten an den μ-,δ- und κ-Opioidrezeptoren mit einer größeren Affinität an µ-Rezeptoren, was zur Dämpfung der Schmerzwahrnehmung führt. Außerdem tragen die Hemmung der Wiederaufnahme von Noradrenalin in das Neuron und die Verstärkung der Serotonin-Freisetzung zu seiner analgetischen Wirkung bei. Hieraus erklärt sich auch die antidepressive und anxiolytische Wirkung, die bei einer Schmerztherapie nicht unerwünscht ist. Auch das vermehrte Auftreten von Übelkeit wird durch die verstärkte Serotonin-Freisetzung erklärt.
Metabolite (1R,2R)-Nortramadol (links) und (1S,2S)-Nortramadol (rechts)
Tramadol wird industriell rein synthetisch hergestellt.[4] Die beiden Enantiomeren des Tramadols und deren Metabolite, insbesondere die am Sauerstoff demethylierten Derivate (Nortramadole), besitzen unterschiedliche pharmakologische Wirkung [μ-Opioid-Bindung Ki(μM)]:[4]- (1R,2R)-Tramadol: 5,1
- (1S,2S)-Tramadol: 120
- (1R,2R)-Nortramadol: 0,02
- (1S,2S)-Nortramadol: 1,8
Hervorzuheben ist noch die geringe organotoxische Wirkung von Tramadol (und Opioiden allgemein); ganz im Gegensatz zu entzündungshemmenden Schmerzmitteln wie NSAR, die in hohem Maße Magen, Darm und andere Organe schädigen können. Auf jeden Fall zu beachten ist allerdings die mit bis zu 30 % recht hohe Non-Responder-Rate.
Tramadol wird bei oraler Gabe zu etwa 95 % resorbiert. Die orale Bioverfügbarkeit wird mit 60 bis 75 % und die Plasmahalbwertszeit mit etwa 5 bis 6 Stunden angegeben.
Nebenwirkungen
Nebenwirkungen wie Schwitzen, Sedierung und Verwirrtheit können auftreten, ebenso wie Schläfrigkeit. In therapeutischer Dosierung hat Tramadol wegen seiner geringen μ-Selektivität keinen beachtenswerten Einfluss auf die Atmung und den Pulmonalarteriendruck. Häufig wird eine starke Übelkeit beobachtet sowohl bei oraler Gabe, als auch bei zu schneller Injektion. Blutdruck und Pulsfrequenz werden kaum beeinflusst.
Bei der Einnahme von mehreren Opioiden wird Tramadol meistens verdrängt, da die meisten anderen Opioide höhere Affinitäten zu den Opioidrezeptoren haben.
Wechselwirkungen mit anderen Medikamenten
Tramadol darf nicht zusammen mit Bupropion (Zyban®) und MAO-Hemmern verwendet werden, es sind schwerwiegende Nebenwirkungen zu erwarten. Bei der Komedikation mit oralen Antikoagulantien[5] ist Vorsicht geboten, und auf den Konsum von Alkohol sollte während der Behandlung verzichtet werden.
Bei der kombinierten Gabe von Tramadol und einem Benzodiazepin muss besondere Vorsicht und eine ununterbrochene Überwachung gewährleistet sein, da beide Stoffgruppen als Nebenwirkung das Atemzentrum dämpfen und so zum Atemstillstand führen können.
Ebenfalls ist große Zurückhaltung geboten, wenn Tramadol mit anderen serotoninergen Medikamenten eingesetzt wird, da es zu einem Serotonin-Syndrom kommen kann.[6] Zu diesen Mitteln zählen auch SSRI-Antidepressiva wie z.B. Fluoxetin und Citalopram und zudem auch illegale Drogen wie Ecstasy und Kokain. Auch rezeptfreie Zubereitungen aus Johanniskraut (Johanniskrauttee, Johanniskrautextrakt in Kapseln usw.) können ein Serotonin-Syndrom auslösen, weswegen der verschreibende Arzt auf die Einnahme derartiger Produkte unbedingt hingewiesen werden sollte. Das Absetzen von Johanniskrautpräparaten unmittelbar vor der Tramadol-Einnahme ist nicht ausreichend, da die serotoninerge Wirkung des Johanniskrauts mehrere Tage anhalten kann.
Tramadol-Injektionslösungen sind inkompatibel, wenn sie in der gleichen Spritze mit parenteralen Darreichungsformen von Diazepam, Diclofenac, Flunitrazepam, Glyceroltrinitrat, Indometacin, [[DL-Lysinmono(acetylsalicylat)]], Midazolam, Piroxicam und Phenylbutazon aufgezogen werden; es kommt zur Ausflockung.[7]
In fixer Kombination wird Tramadol mit Paracetamol als Zaldiar® 37,5 mg/325 mg von Grünenthal GmbH angeboten.
Gewöhnung und Abhängigkeitspotential
Eine psychische Abhängigkeit kann bei längerfristigem, selten auch bei kurzfristigem Konsum eintreten. Körperliche Abhängigkeit tritt nur selten auf.
Die Einnahme über einen längeren Zeitraum kann zu einer akkumulierten Freigabe von Dopamin und Noradrenalin führen, sobald das Medikament abgesetzt wird. Dies kann in den ersten zwei bis drei Wochen nach Absetzen zu verstärktem Schmerzempfinden und Unwohlsein führen.
Das Suchtpotential bei Missbrauch von Tramadol ist erheblich. In der Ukraine entwickelte sich Tramadol 2004 in kurzer Zeit zu einer der wichtigsten Einstiegsdrogen. Von den in der Ukraine jährlich produzierten 90 Millionen Packungen Tramadol werden nur etwa 5 Millionen regulär von Patienten verbraucht, während etwa 85 Millionen Packungen aller Wahrscheinlichkeit nach dem illegalen Konsum und dem Schmuggel in andere Länder zufließen.[8] Inoffiziellen Daten zufolge haben bereits zwei Drittel der ukrainischen Schüler im Alter von zwölf Jahren und älter Tramadol konsumiert.[9] Der Dokumentarfilm "Am Rande - Sechs Kapitel über AIDS in der Ukraine" von Karsten Hein aus dem Jahr 2006 beschäftigt sich auch mit der Bedeutung von Tramadol als Einstiegsdroge in einem Land, in dem die epidemisch verbreitete Drogensucht die Hauptursache einer AIDS-Epidemie ist.[10]
Chemie und Isomerie
Die chemische Synthese von Tramadol ist in der Literatur[11] beschrieben. Tramadol [2-(Dimethylaminomethyl)-1-(3-methoxyphenyl)cyclohexanol] besitzt zwei stereogene Zentren am Cyclohexanring. Von 2-(Dimethylaminomethyl)-1-(3-methoxyphenyl)cyclohexanol gibt es also vier Konfigurationsisomere: (1R,2R)-Form (1S,2S)-Form, (1R,2S)-Form und die (1S,2R)-Form. Bei der Synthese entstehen die (1R,2R)-Form und die (1S,2S)-Form als Hauptprodukt in gleicher Menge. In geringerer Menge wird bei der Synthese das Racemat aus der (1R,2S)-Form und der (1S,2R)-Form gebildet. Die Isolation der (1R,2R)-Form und (1S,2S)-Form und somit des Abtrennung des Nebenprodukt-Racemates aus (1R,2S)-Form und der (1S,2R)-Form gelingt über die fraktionierende Kristallisation der Hydrochloride. Der Arzneistoff Tramadol ist als Racemat aus der (1R,2R)-Form und der (1S,2S)-Form als Hydrochlorid im Handel (Tramal®).
Die Trennung des Racemates aus der (1R,2R)-Form und der (1S,2S)-Form mit (R)-(−)- oder (S)-(+)-Mandelsäure ist in der Literatur[12] beschrieben, findet jedoch keine industrielle Anwendung, da Tramadol als Enantiomerengemisch benutzt wird, obwohl die unterschiedliche physiologische Wirkung der (1R,2R)- und (1S,2S)-Enantiomere belegt[13] ist.
Das Hydrochlorid des Racemates aus der (1R,2R)-Form und der (1S,2S)-Form, das Grünenthal in Deutschland als Pharmawirkstoff entwickelte, wurde im ursprünglichen Patent[14] und in den allermeisten Veröffentlichungen [15] fälschlicherweise als das (±)-trans-Tramadol beschrieben. Im Zuge des Zulassungsverfahrens in den Vereinigten Staaten wurde der Name in (±)-cis-Tramadol geändert[16]. Alternativ kann der racemische Arzneistoff (±)-cis-Tramadol auch als (±)-(1R*,2R*)-Tramadol bezeichnet werden, wobei mit (1R*,2R*) die realative Stereochemie angegeben ist, es sich also um ein Gemisch der (1R,2R)-Form und der (1S,2S)-Form handelt.
Quellen
- ↑ a b Tramadol bei DrugBank
- ↑ a b Sicherheitsdatenblatt für Tramadol-Hydrochlorid – Sigma-Aldrich 09.12.2007
- ↑ Tramadol bei ChemIDplus
- ↑ a b Bernd Schäfer: Naturstoffe der chemischen Industrie, Elsevier, 2007, S. 255.256, ISBN 978-3-8274-1614-8.
- ↑ Scher ML, et al. Potential interaction between tramadol and warfarin. Ann Pharmacother 1997; 31: 646–7
- ↑ Woggon, Brigitte (2005) Behandlung mit Psychopharmaka (2. Auflage). Bern: Hans Huber. ISBN 3-456-83538-8
- ↑ Abanmy NO, et al. Compatibility of tramadol hydrochloride injection with selected drugs and solutions. Am J Health-Syst Pharm 2005; 62: 1299–1302
- ↑ http://www.kyivpost.com/nation/28813/
- ↑ http://www.kyivpost.com/nation/28813/
- ↑ http://www.aids-ukraine.com/am-rande/index.html)
- ↑ Pharmaceutical Substances, Axel Kleemann, Jürgen Engel, Bernd Kutscher und Dieter Reichert, 4. Auflage (2000) 2 Bände erschienen im Thieme-Verlag Stuttgart, dort Seiten 2085 bis 2086, ISBN 978-1-58890-031-9; seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen.
- ↑ Zynovy Itov und Harold Meckler: A Practical Procedure for the Resolution of (+)- and (−)-Tramadol, Organic Process Research & Development 2000, 291-294.
- ↑ D. Burke und D. J. Henderson: Chirality: a blueprint for the future, British Journal of Anaesthesia 88 (2002) 563-576.
- ↑ (a) K. Flick und E. v. Frankus, U.S. Patent 3 652 589 (Grünenthal GmbH) 28. März 1972; Chemical Abstracts 76 (1972) 153321. (b) K. Flick und E. Frankus, U.S. Patent 3 830 934 (Grünenthal GmbH) 20. August 1974; Chemical Abstracts 82 (1974) 21817
- ↑ Beispiele: E. v. Frankus, E. Friedrichs, S. M. Kim und G. Osterloh, Arzneimittel-Forschung / Drug Research 28 (1978) 114-121. (b) K. Flick, E. v. Frankus und E. Friedrichs, Arzneimittel-Forschung / Drug Research 28 (1978) 107-113. (c) Y. A. Ardakani und M.-R. Rouini, Journal of Pharmaceutical and Biomedical Analysis 44 (2007) 1168-1173.
- ↑ Physicians Desk Reference; Medical Economics Data, Oradell, N.J., 54 (2000) 2218–2219.
Weblinks
- Tramadol bei Erowid (englisch)
- arznei-telegramm (1/2002): Serotonin-Syndrom unter Analgetikum Tramadol (Tramal u.a.)
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.